
刚刚过去的8月,国家药品监督管理局药品审评中心(CDE)更新了一批细胞治疗药物的受理动态。从最新名单中可以看出一个明显趋势:免疫细胞与干细胞药物双双迈进,这不仅反映出我国细胞与基因治疗(CGT)领域的研发活力,也预示着未来肿瘤和慢性疾病的治疗选择将更加丰富。
NK、TIL疗法临床受理升温
在本期免疫细胞疗法进展中,NK细胞与TIL疗法同时获得受理。NK细胞因其不需特异识别即可广泛攻击肿瘤或病毒感染的细胞,常被称为“天然杀手”。而TIL疗法则侧重于提取肿瘤组织内已有的淋巴细胞,经体外扩增后回输至患者体内,类似于激活体内已有的“免疫战队”。这两类产品同时进入审评程序,表明国内在肿瘤免疫治疗,尤其是实体瘤领域的研究正在持续推进。
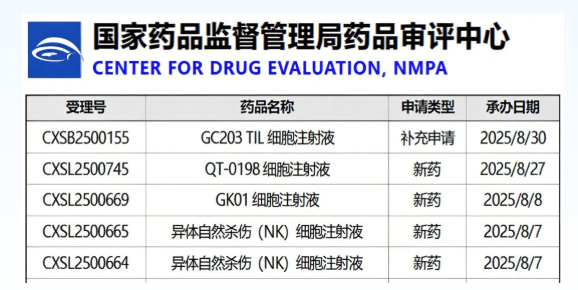
MSC药物获受理,瞄准多病种修复
2025年中国干细胞临床研究迎来爆发式增长。截至5月,全国已有148家医疗机构完成备案,启动133项临床研究,覆盖50多种重大疾病,重点攻坚神经、心血管、免疫等领域难治性疾病。干细胞不直接杀伤肿瘤,却以优异的免疫调节与组织再生能力,为缺乏治疗手段的患者带来新希望。
除免疫细胞外,间充质干细胞(MSC)也有新药申报获得受理。MSC不像NK和TIL那样侧重直接攻击肿瘤,而更专注于组织修复与免疫调节,可形象比喻为“修复工程师”,在缓解炎症、促进组织再生等方面发挥作用。近年来,MSC在骨关节炎、心脏病、神经损伤等多种疾病中的应用不断拓展,新申报项目进一步体现了其临床潜力被持续看好。

创新与迭代同步爆发
从受理类型来看,此次既有全新药物申请,也包括对已上市产品的补充申请。新药申报代表新的研发方向和探索不断涌现,补充申请则意味着已有产品在工艺、适应症或使用方法方面持续优化。这一点反映出细胞治疗药物已逐步脱离早期研究阶段,进入更加成熟、规范、可持续发展的新周期。
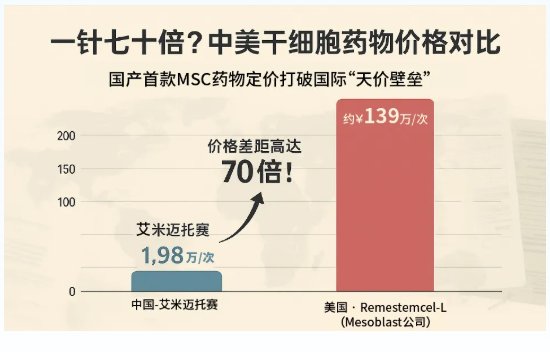
回顾2025年6月5日,中国干细胞医疗迎来重大突破:国内首款间充质干细胞药物——艾米迈托赛注射液(商品名:睿铂生),由铂生卓越生物科技(北京)研发,在北京大学人民医院完成全国首例应用,用于治疗14岁以上激素无效的急性移植物抗宿主病(aGVHD)。

该药单支定价仅19800元(规格12mL,含6×10^7个细胞),不足国际同类产品价格的七十分之一,以“颠覆性低价”大幅降低治疗门槛。与此同时,301医院也宣布布局三条干细胞新赛道,推动临床转化全面加速。
将NK、TIL与MSC三类细胞药物并列观察,可以看出当前行业发展的双主线:免疫细胞疗法主攻肿瘤治疗,研发节奏快、突破频出;干细胞则侧重于慢性病和组织修复领域,强调稳健积累与长期价值。两者互补并进,为未来细胞治疗的应用开辟了更立体的格局,也有望为不同健康状况的患者提供更多治疗选择。
综述
8月的细胞药物受理信息,不仅是一批审批编号的更新,更是整个行业加速发展的一个侧影。从精准对抗肿瘤的免疫细胞,到多方修复损害的干细胞,我们可以清晰看到:细胞药物正在越来越多地从实验室研究走向临床实际应用,未来医疗的可能性正在不断扩展
欢迎关注微信公众平台:重庆铂而斐
免责声明: 我们尊重原创,也注重分享,不作商业用途,不作医疗建议,仅作交流学习。版权归原作者,如有侵权敬请谅解,请联系我们删除。